Cette protéine fait partie des plus étudiées dans le Chembl: CHEMBL2041. Le site a été défini à l’aide du PDB 2IVU.

Vue de référence utilisée par la suite pour présenter les résultats.
Etude des ligands les plus actifs
Molécule n°1

smiles: CC(C)n1nc(-c2noc(C3CC3)c2-c2ccccn2)c2c(N)ncc(Cl)c21
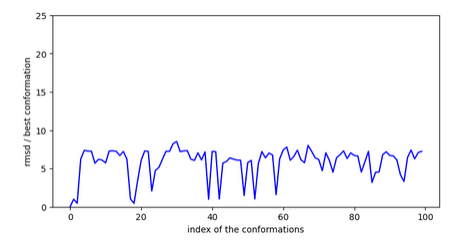
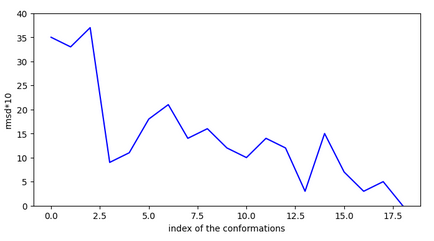
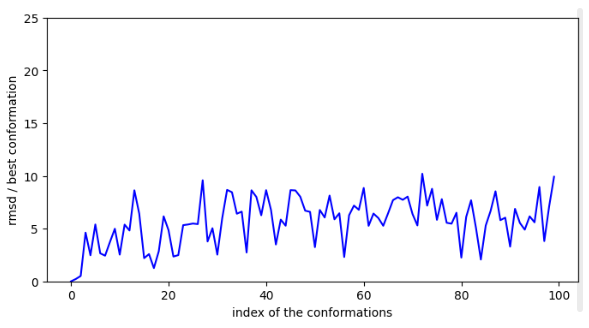
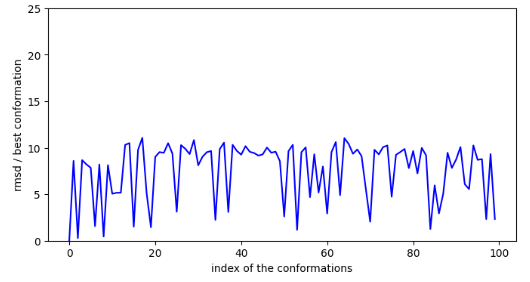
rmsd des conformations par rapport à la plus stables.
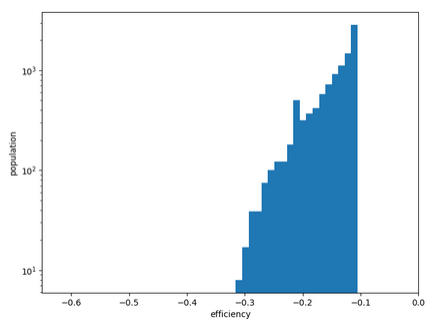
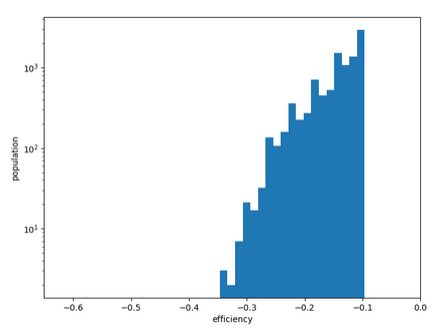
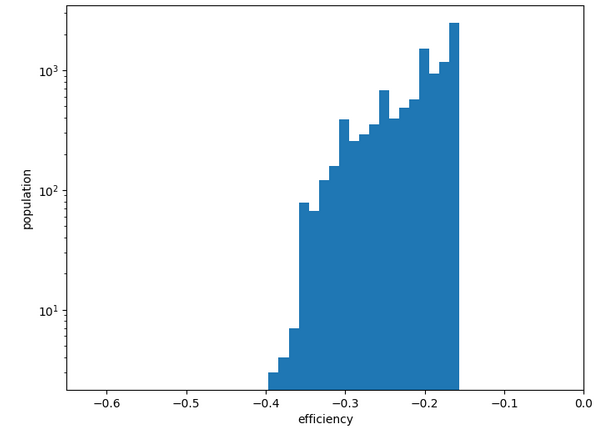
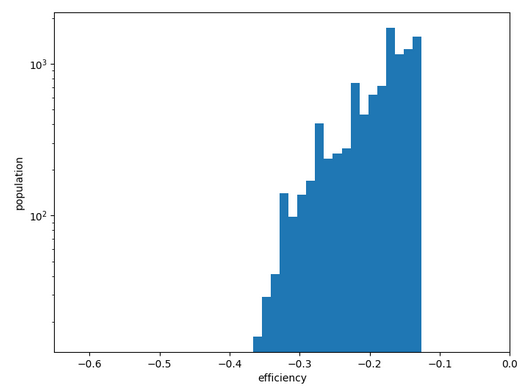
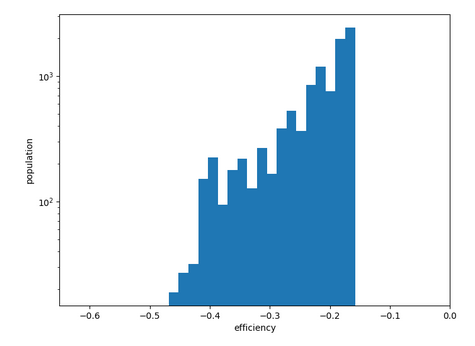
Distribution des conformations en fonction du score SMINA. Limitation aux 10_000 meilleures.
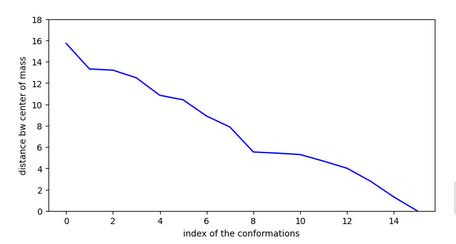
Chemin n°1:
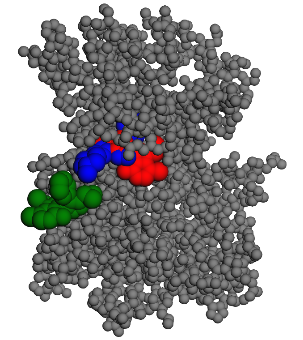
En vert la conformation initiale.
En rouge la conformation finale.
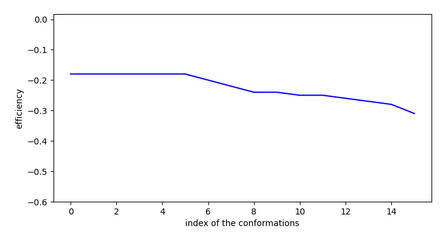
Molécule n°2

smiles:Cc1cc(NC(=O)c2c(C#CC3(O)CCCC3)n(C3(C)CC3)c3ncnc(N)c23)n[nH]1
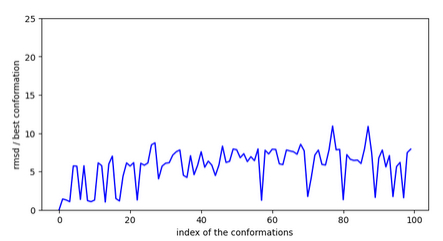
Chemin n°1
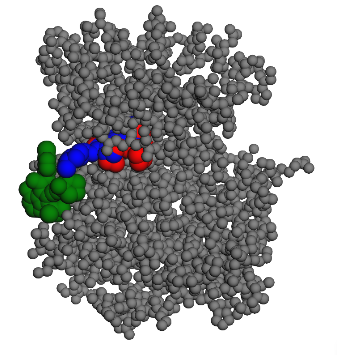
Toutes les solutions sont similaires à celle-ci.
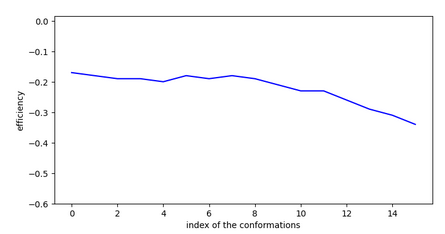
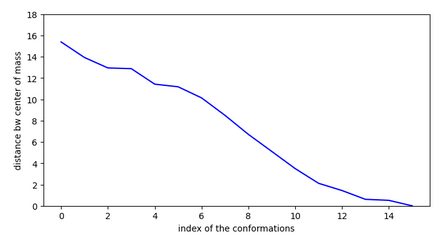
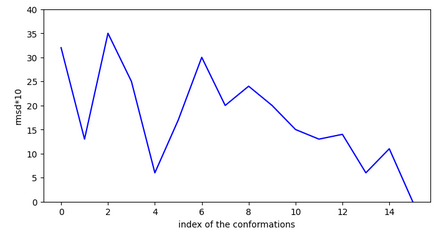
Etudes des ligands inactifs
Molécule n°1

smiles: O=C(O)c1cccc2[nH]c(-c3n[nH]c4ncc(-c5cncc6ccccc56)cc34)nc12
Chemin n°1:
Les 15 premières conformations testées ne sont pas connectées à une conformation en surface
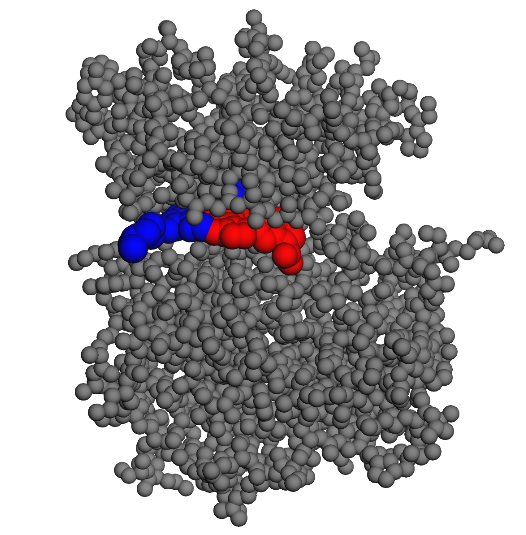
Cette molécule ne fonctionne pas car, à priori, elle ne trouve pas de chemin depuis la surface jusqu’à sa conformation stable.
Molécule n°2:
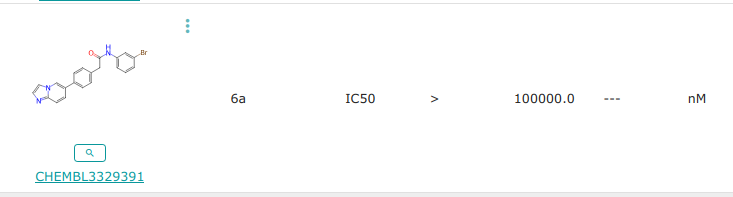
smiles: O=C(Cc1ccc(-c2ccc3nccn3c2)cc1)Nc1cccc(Br)c1
Chemin n°1:
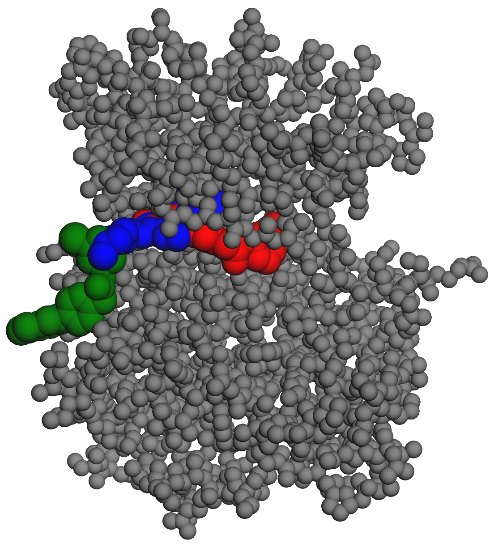
A priori, ici le problème est différent, ce ligand n’est pas actif car il doit faire un ou des sauts impossibles à réaliser entre conformations stables.
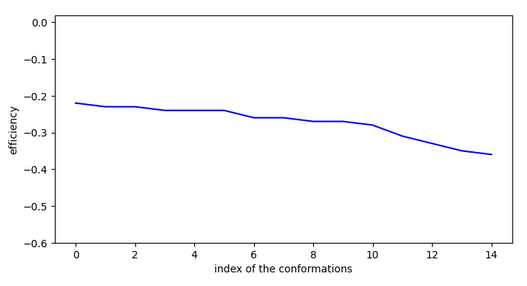
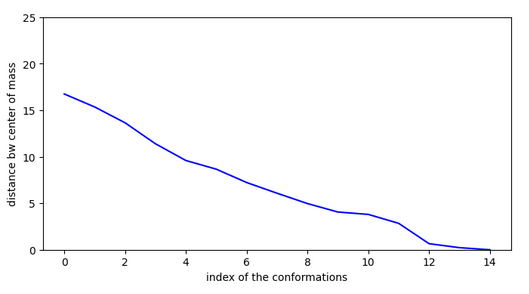
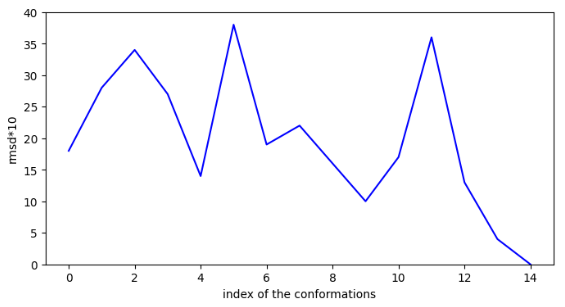
Molécule n°3:
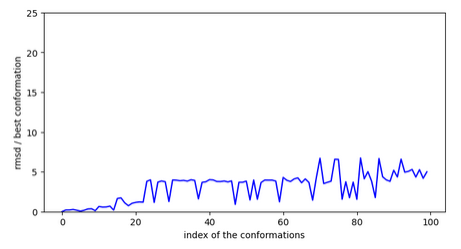
Chemin n°1
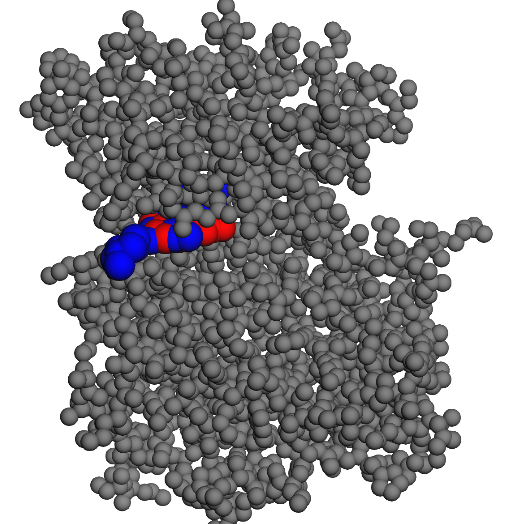
La molécule trouve une conformation très stable dans la cavité mais il n’y a pas de chemin pour y accéder depuis la surface! La vérification a été faite sur les 15 conformations les plus stables.

