Objectif
Afin de prouver la capacité d’Emolgine à proposer des molécules pertinentes pour les récepteurs nicotinic de l’acéthylcholine, nous avons convenu de choisir une cible très connue, le récepteur nicotinique humain alpha 7 de l’acetylcholine et de trouver une molécule disponible dans le commerce qui soit un antagoniste efficace non connu.
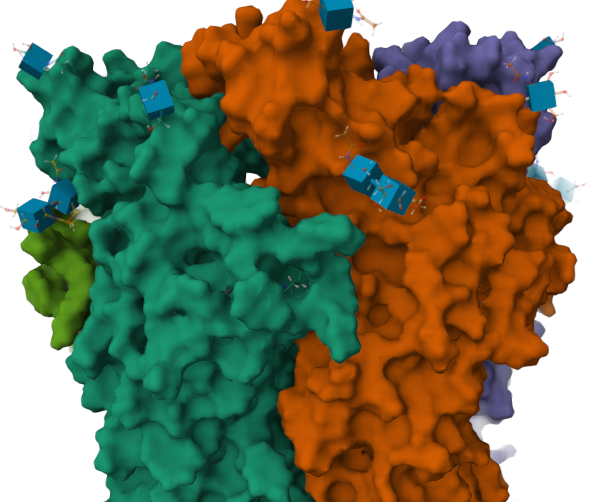
Le PDB 7KOQ a été utilisé pour définir le site. La vue ci-contre sera utilisée pour présenter les résultats.
Résutats expérimentaux dans la Chembl
Il y a 3 références Chembl pour cette protéine:
– CHEMBL4980 pour l’organisme “Rattus norvegicus”;
– CHEMBL3365 pour l’orgnaisme “Mus musculus”;
– CHEMBL5169123 pour l’organisme “Gallus gallus”;
Etude des molécules les plus actives
1

smiles: O=C(N[C@@H]1C2CCN(CC2)[C@@H]1Cc1cccnc1)c1ccc(I)s1
Cette molécule est très intéressante car elles passe d’une grande activité sur alpha 7 à presque rien sur alpha-4 beta-2.
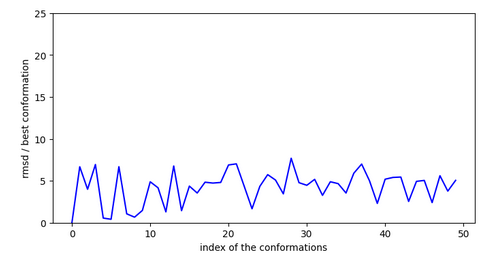
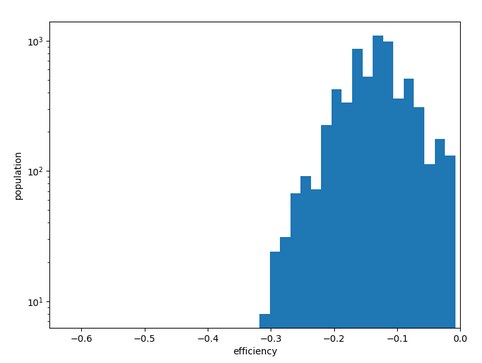
Chemin n°1
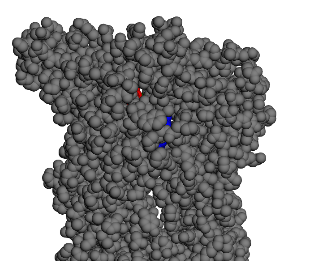
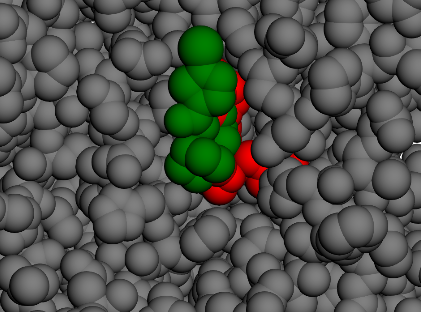
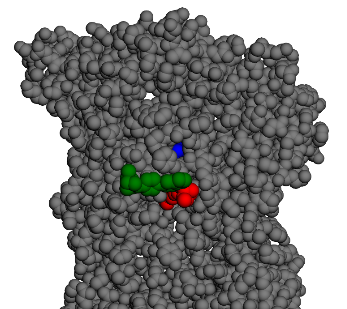
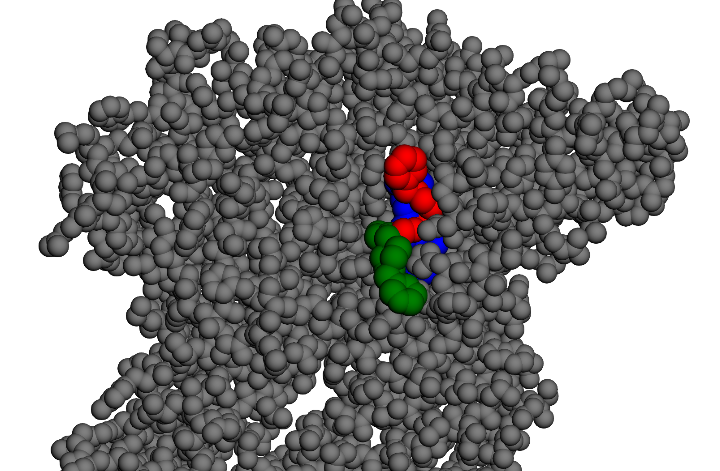
La molécule ne se stabilise pas sur l’extérieur du canal mais à l’intérieur (vue ci-dessous)
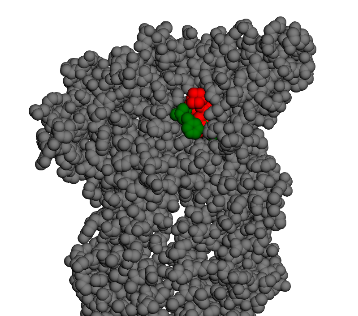
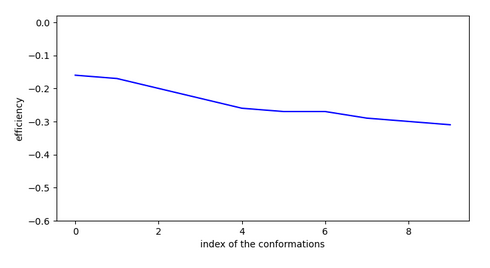
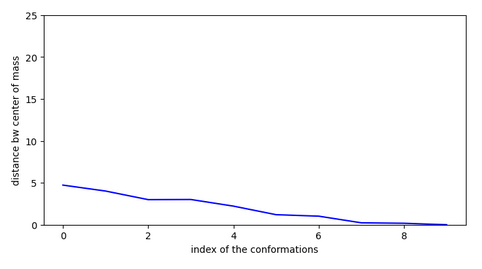
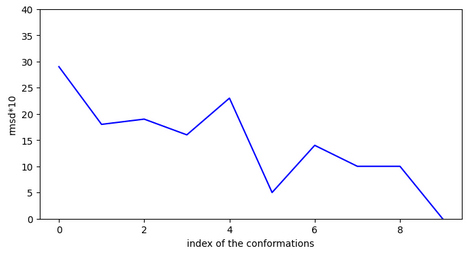
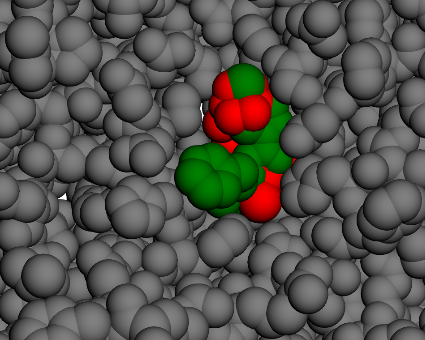
Tous les autres chemins sont similaires. Cette molécule possède 2 conformations stables dans cette cavité au sein du canal ionique:
2
smiles:CN1C[C@@H]2C[C@H]1CN2c1ccc(-c2ccc3[nH]ccc3c2)cn1
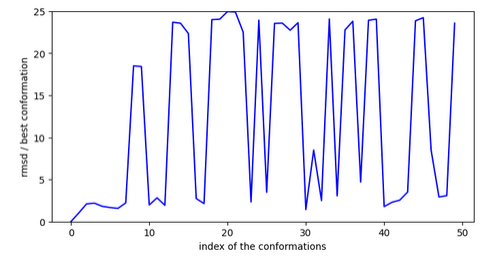
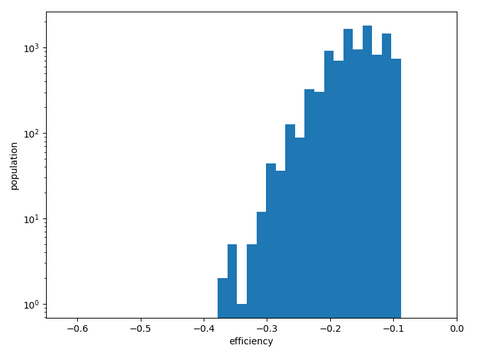
Chemin n°1
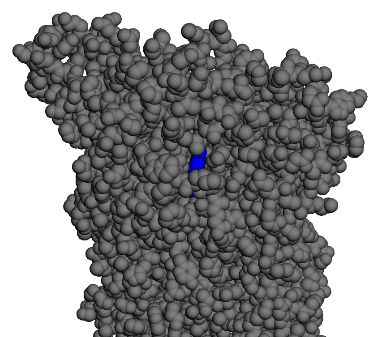
La conformation la plus stable se trouve dans le canal ionique, donc pas visible sur la figure ci-dessus.
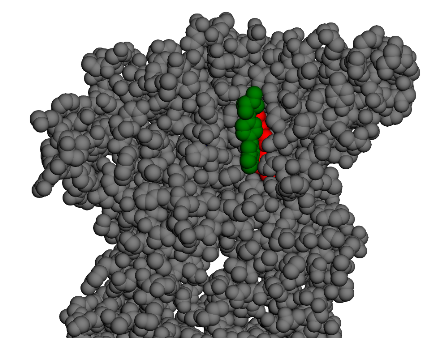
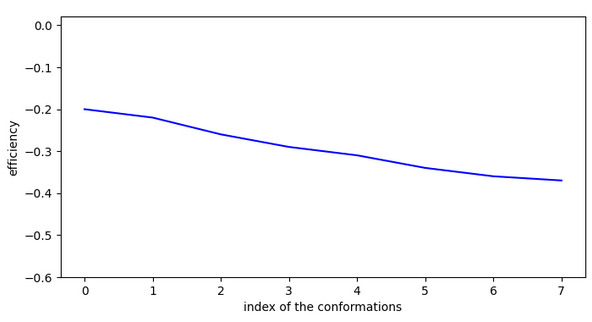
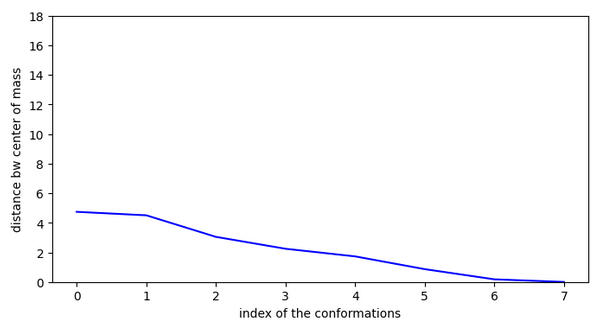
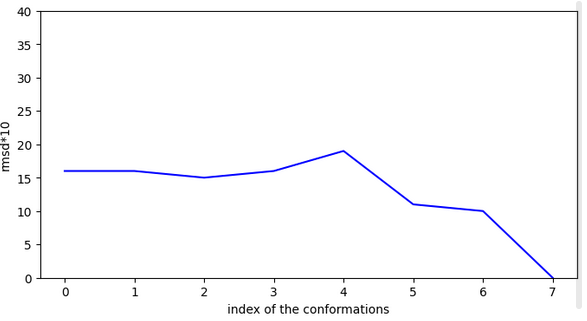
Chemin n°2
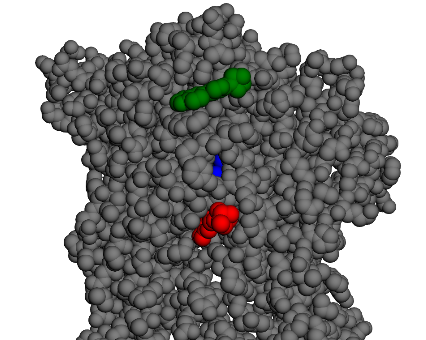
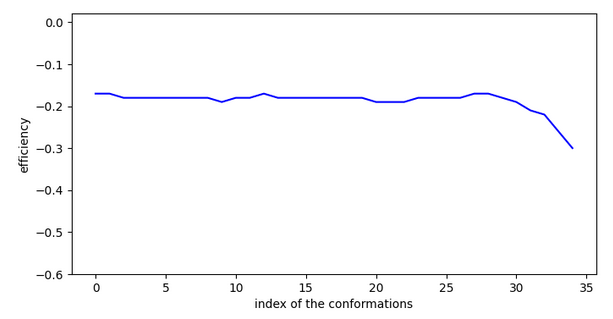
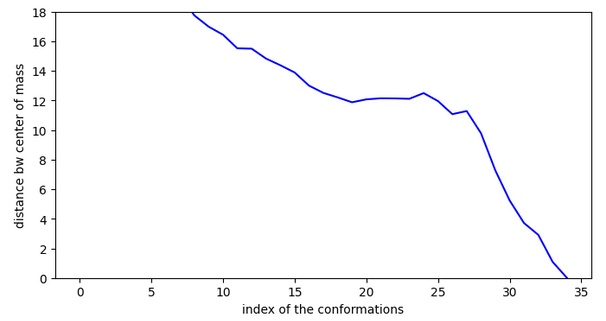
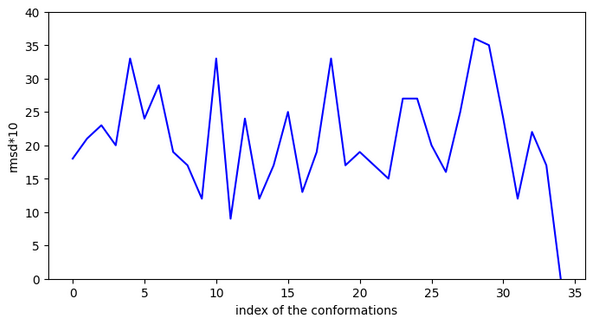
Chemin n°3
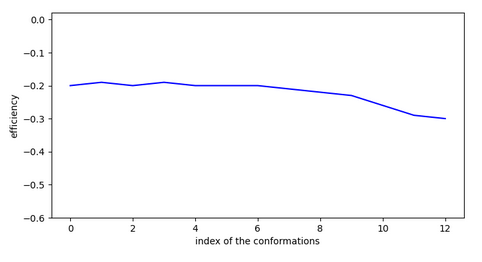
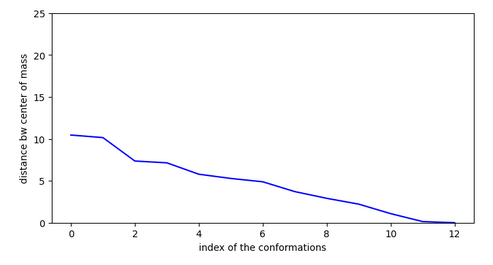
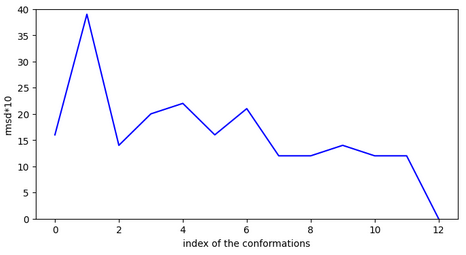
3

O=S1(=O)c2ccccc2-c2ccc(N3CCN4CCC3CC4)cc21
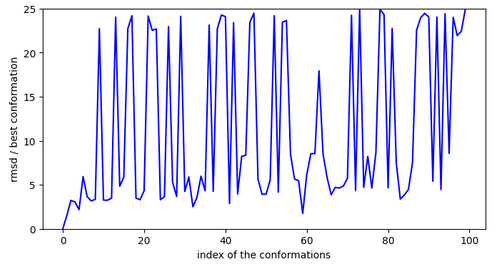
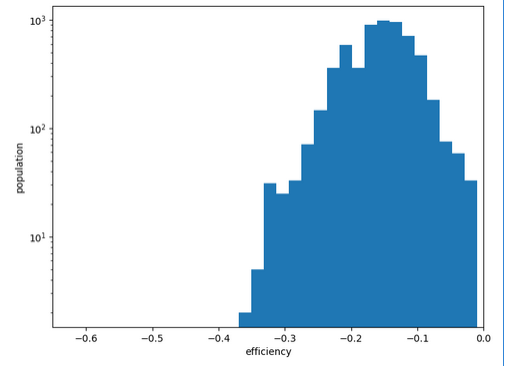
Chemin n°1
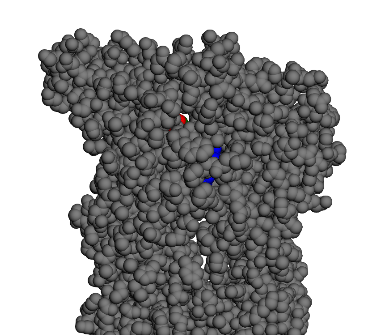
Comme pour les molécules précédentes, la conformation la plus stable n’est accessible depuis l’extérieur mais depuis l’intérieur du canal ionique.
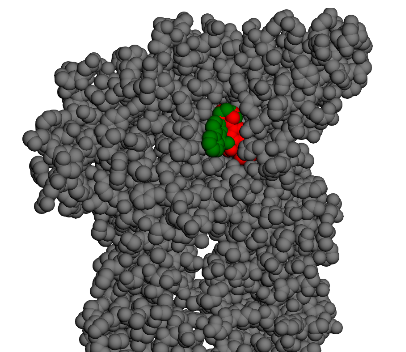
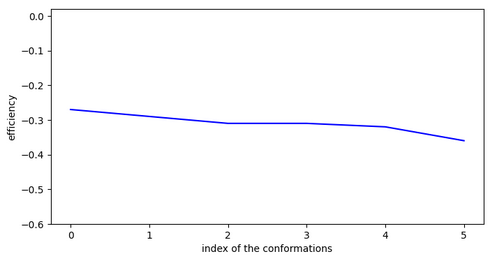
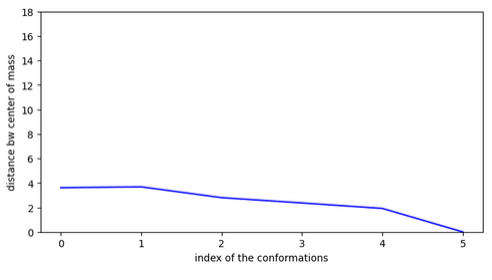
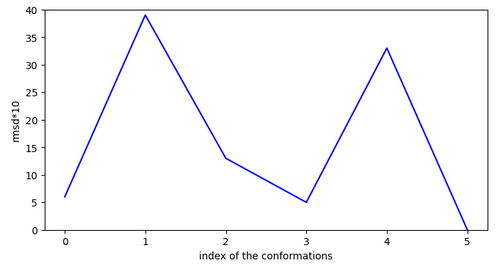
Conclusion: Cet exemple montre clairement qu’une évaluation sur un seul chemin ne suffit pas, il faut étudier toutes les solutions. En effet, pour cette première solution, la molécule fait des sauts trop importants malgré son activité.
Si on se focalise sur le site pour faire un docking, on obtient alors:
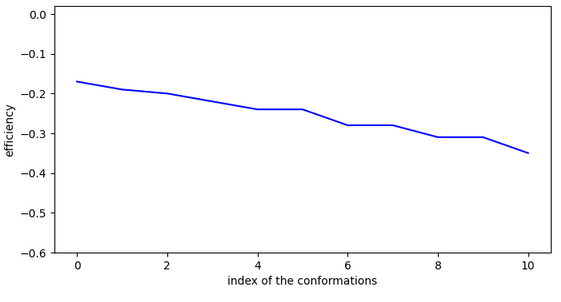
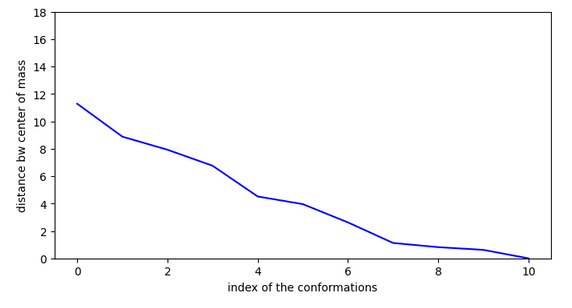
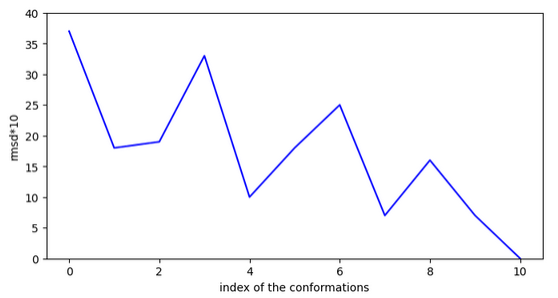
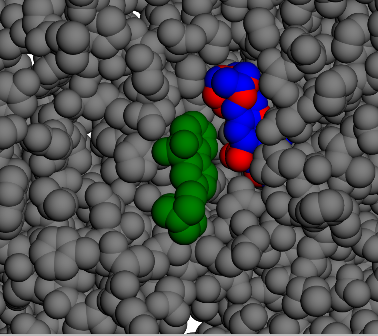
4:
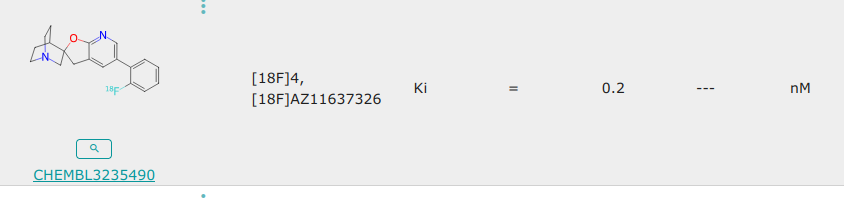
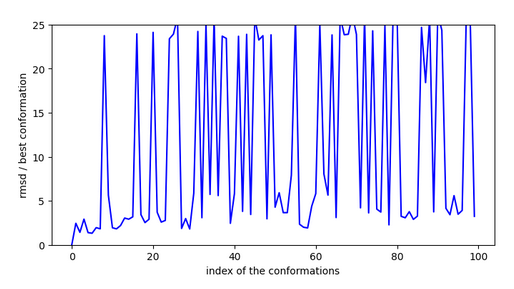
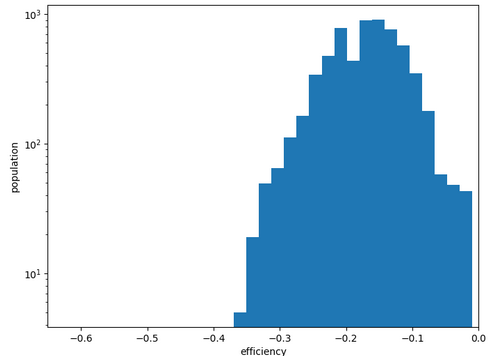
Chemin n°1
Comme pour les molécules précédentes, la conformation la plus stable n’est pas accesible depuis l’extérieur mais depuis l’intérieur.
La deuxième solution de chemin est similaire aux molécules précédentes.
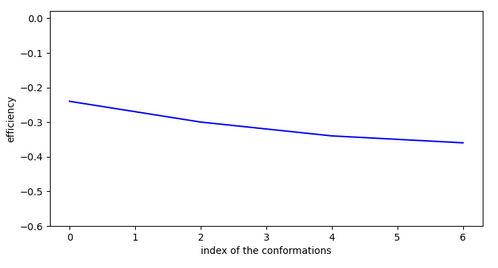
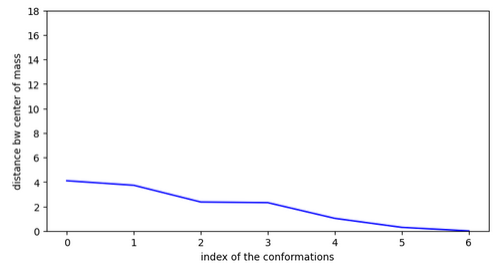
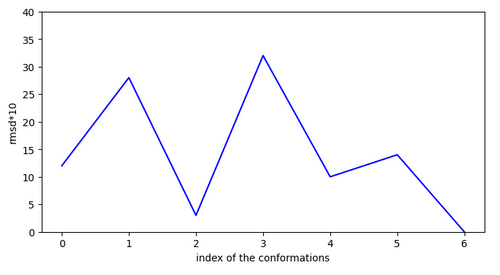
Conclusion à partir des molécules actives
Les molécules les plus actives ne rentrent pas dans la cavité mais en bloque l’accès et ce depuis l’intérieur du canal ionique !
Etude des molécules inactives
–
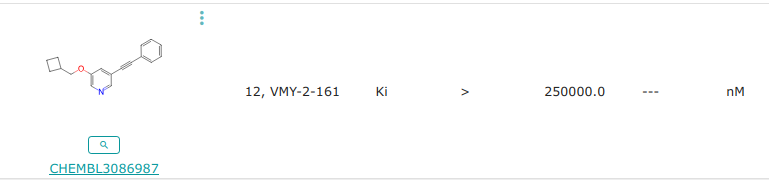
C(#Cc1cncc(OCC2CCC2)c1)c1ccccc1
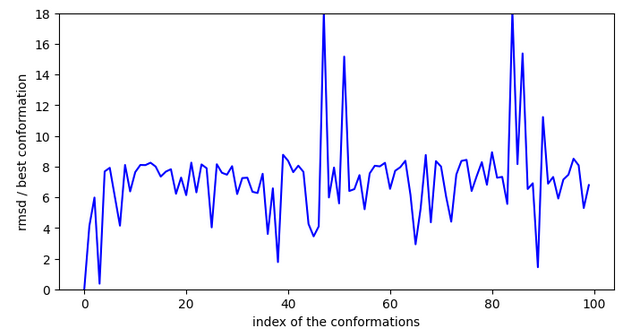
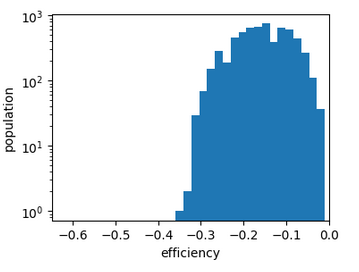
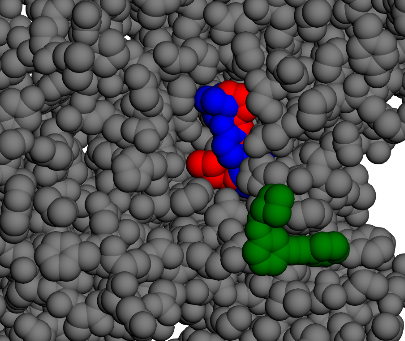
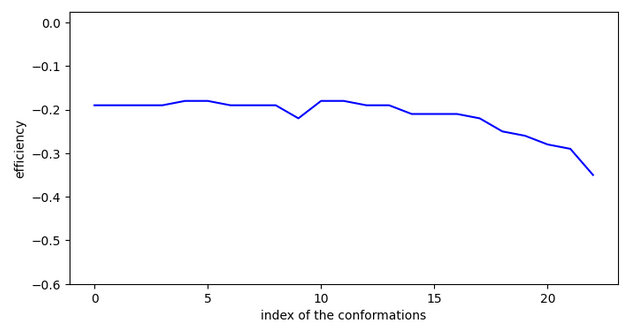
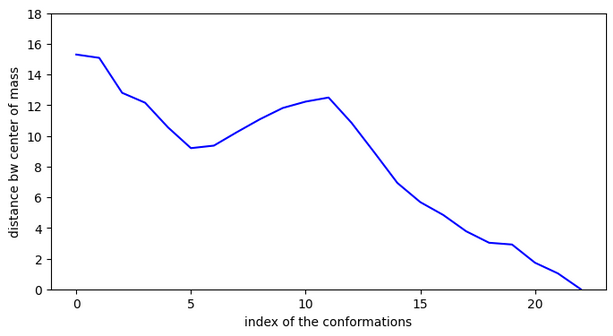
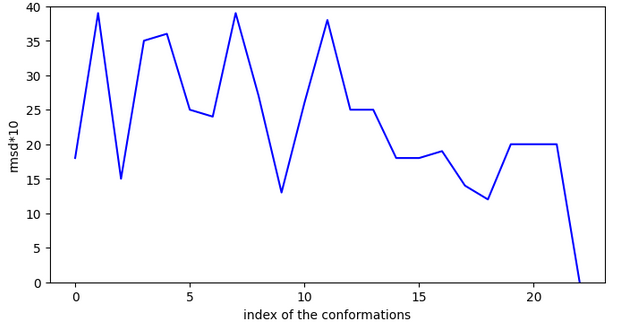
Il est possible que le fait de pouvoir se stabiliser loin de l’entrée de la cavité et de devoir faire des sauts importants pour y rentrer soit négatif.
–
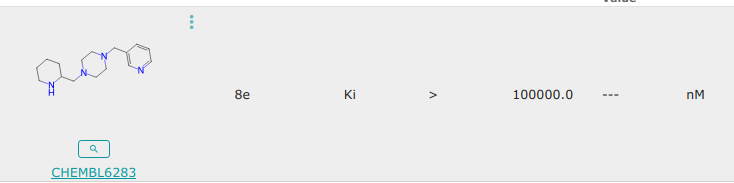
c1cncc(CN2CCN(CC3CCCCN3)CC2)c1
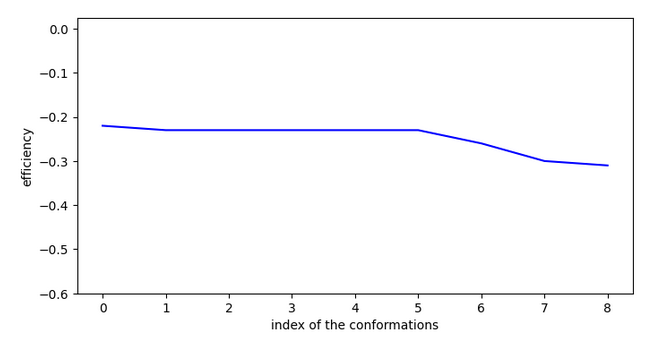
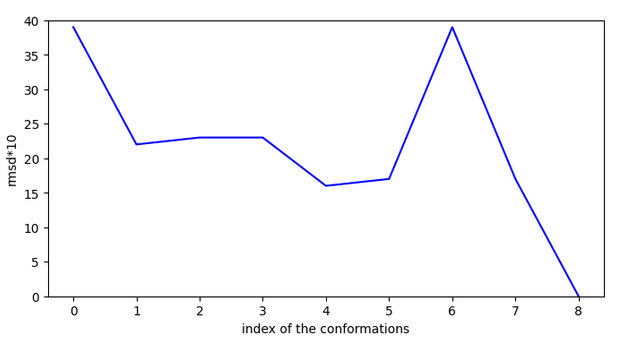
A priori, cette molécule ne marche pas car il y a très peu de descente de potentiel et il y a souvent des sauts importants.
2

CC(CCOC(=O)N1CCCCC1)N(C)C
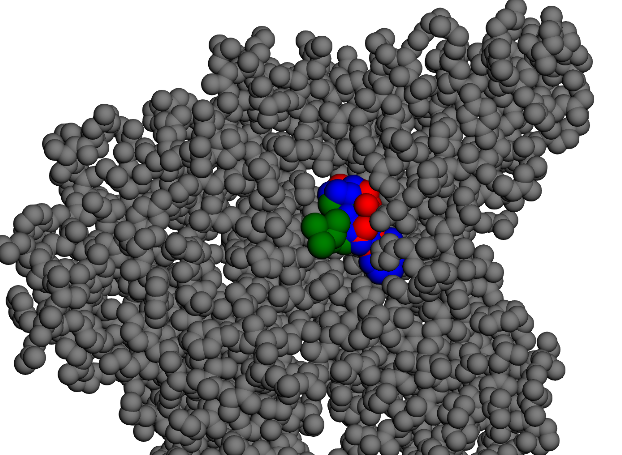
A priori, cette molécule ne fonctionne pas car la conformation initiale ne semble pas assez accessible (trop proche de la conformation finale).
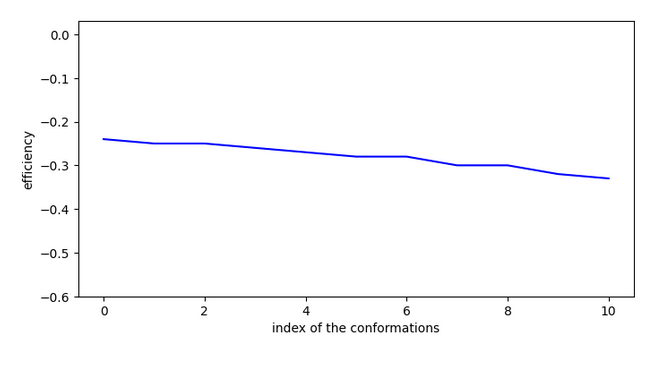
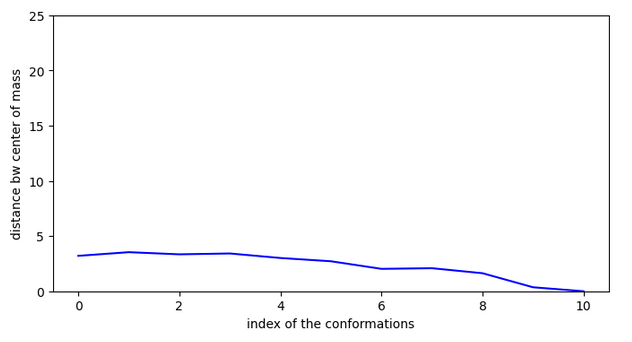
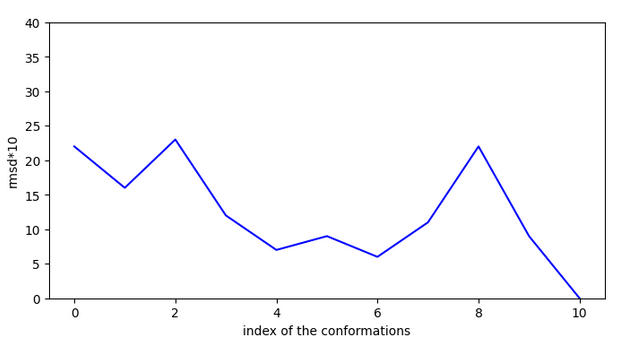
Proposition de molécules
Les molécules suivantes ont été choisies en appliquant la formule suivante (10+logP)*sascore*(1+efficiency). Les molécules testées sont les plus solubles, les plus simples à synthétiser et celles ayant le plus d’affinité.
1 KO
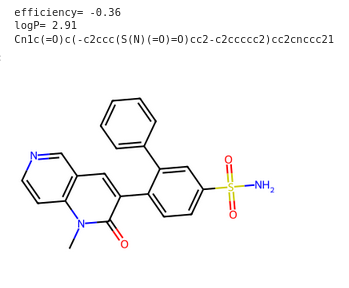
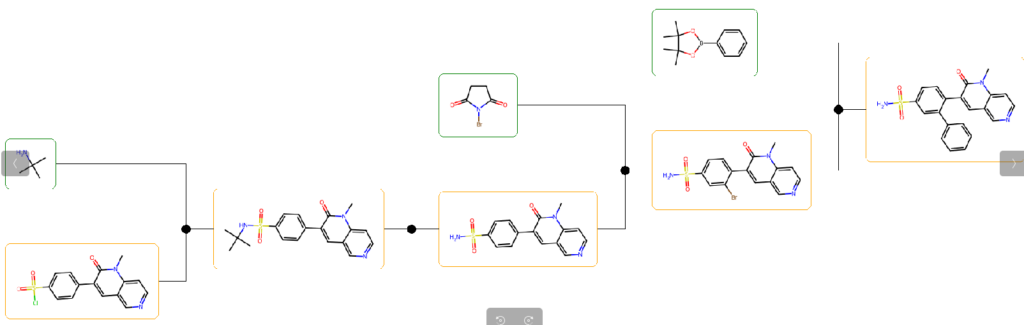
Cn1c(=O)c(-c2ccc(S(N)(=O)=O)cc2-c2ccccc2)cc2cnccc21
Trop complexe à synthétiser.
2 OK
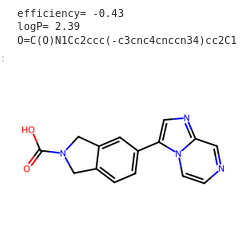
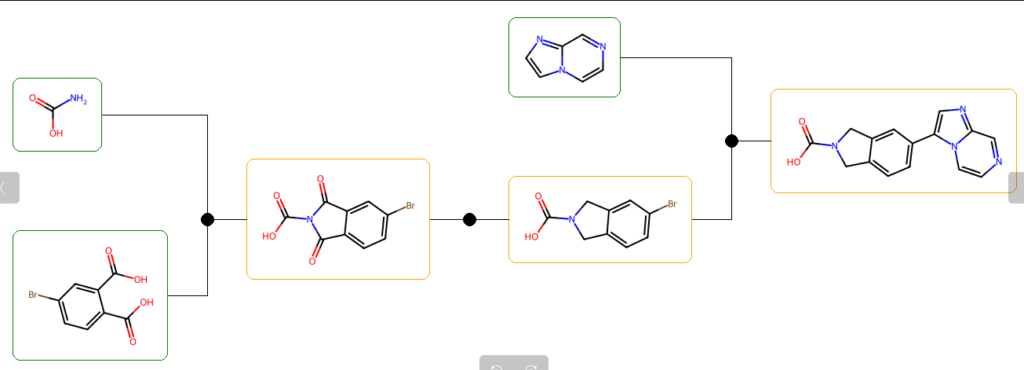
O=C(O)N1Cc2ccc(-c3cnc4cnccn34)cc2C1
3 KO
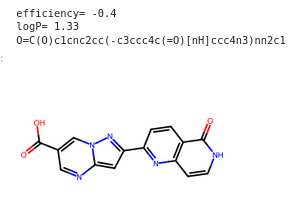
O=C(O)c1cnc2cc(-c3ccc4c(=O)[nH]ccc4n3)nn2c1
Trop complexe à synthétiser.
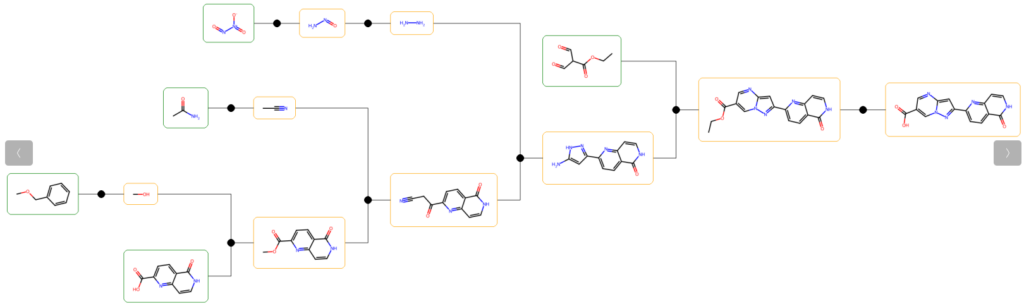
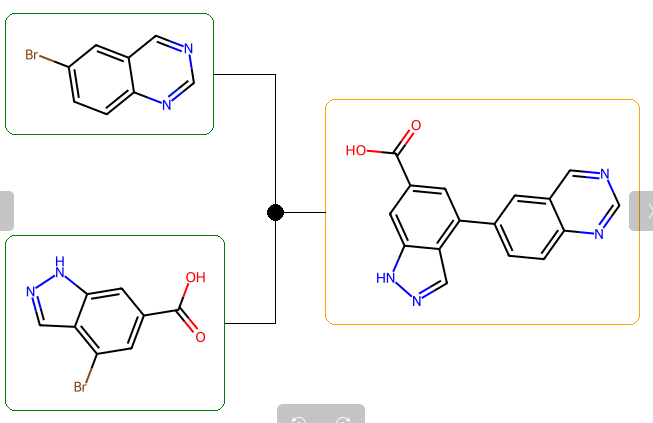
4 OK
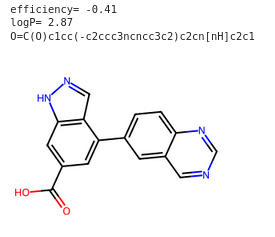
O=C(O)c1cc(-c2ccc3ncncc3c2)c2cn[nH]c2c1
5 KO
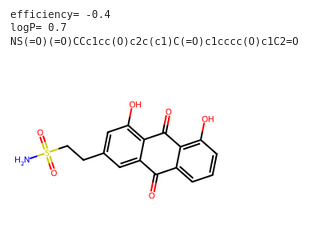
NS(=O)(=O)CCc1cc(O)c2c(c1)C(=O)c1cccc(O)c1C2=O
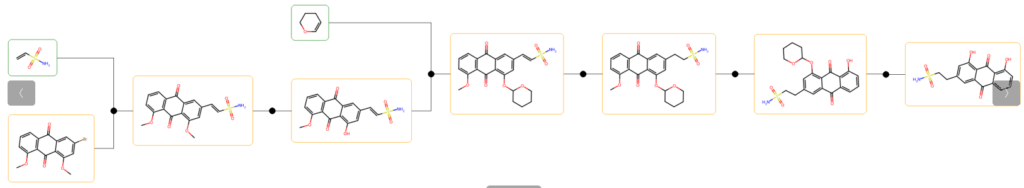
6 OK
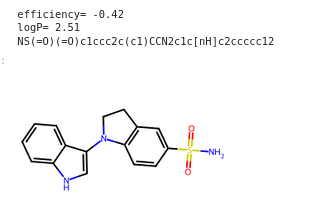
NS(=O)(=O)c1ccc2c(c1)CCN2c1c[nH]c2ccccc12
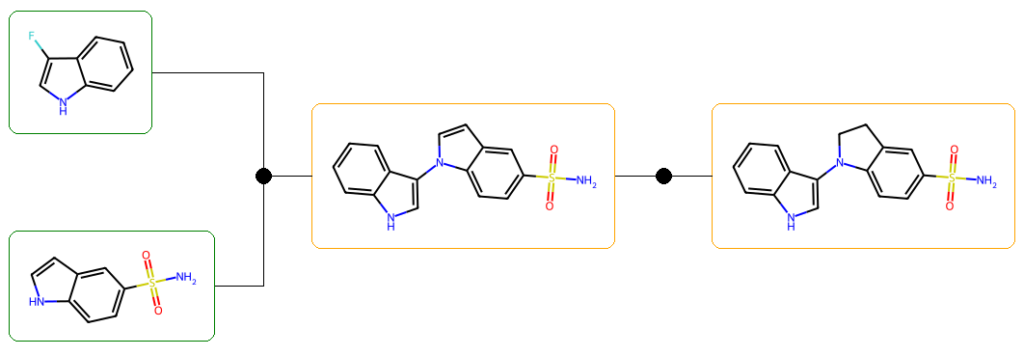
7 OK
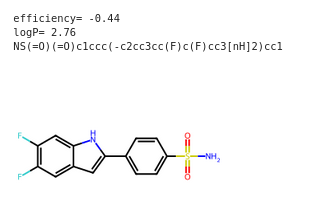
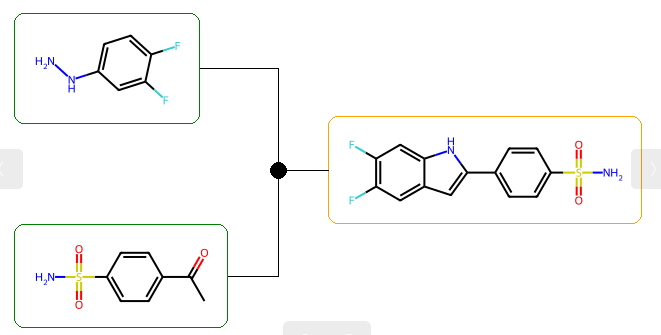
NS(=O)(=O)c1ccc(-c2cc3cc(F)c(F)cc3[nH]2)cc1
8 KO
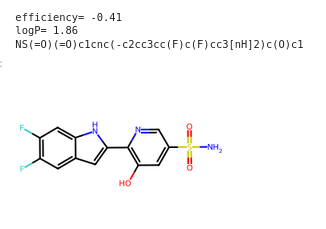
NS(=O)(=O)c1cnc(-c2cc3cc(F)c(F)cc3[nH]2)c(O)c1
9 OK
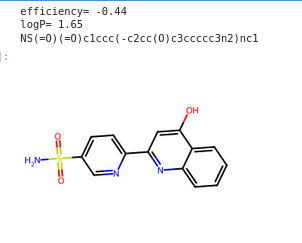
NS(=O)(=O)c1ccc(-c2cc(O)c3ccccc3n2)nc1
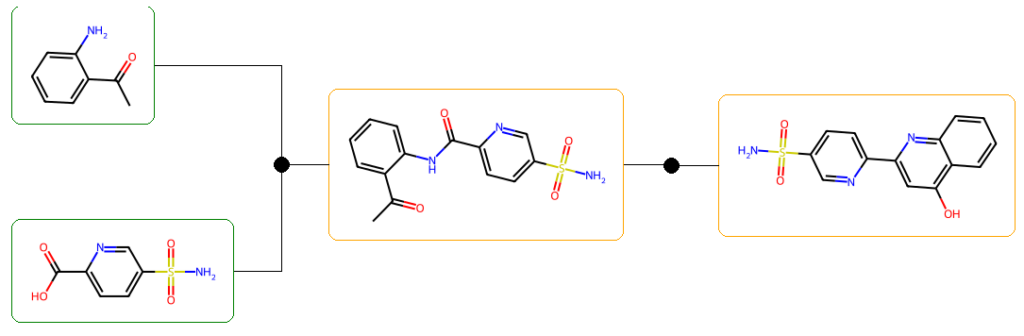
NS(=O)(=O)c1ccc(-c2cc(O)c3ccccc3n2)nc1
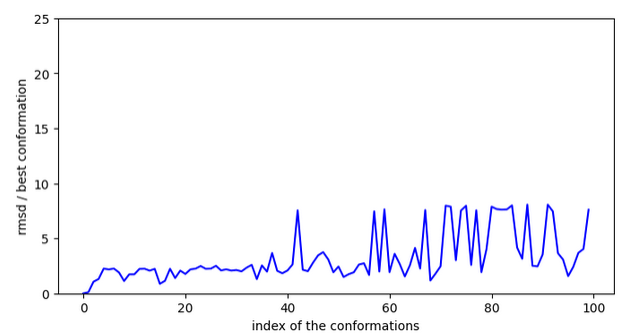
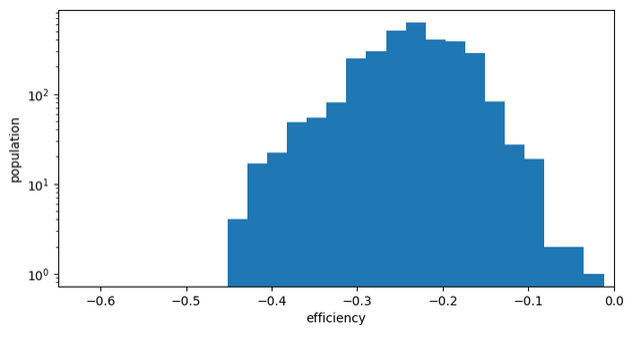
Chemin 1
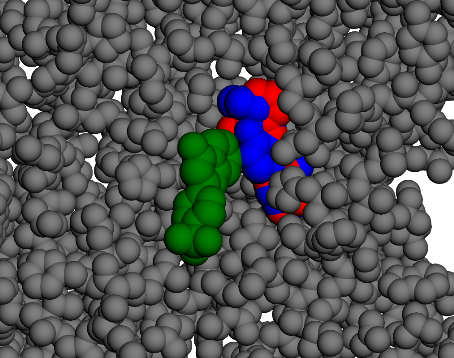
Saut important !
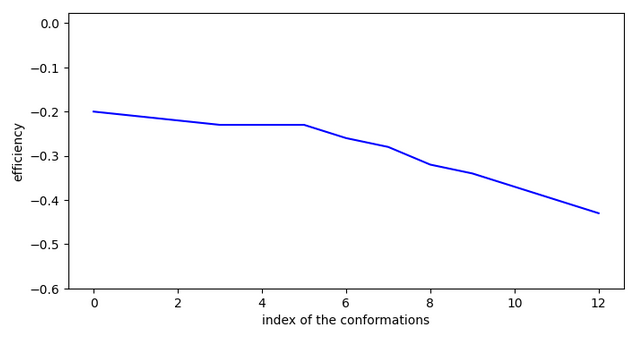
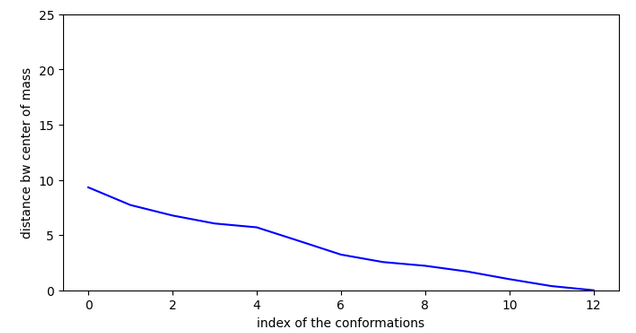
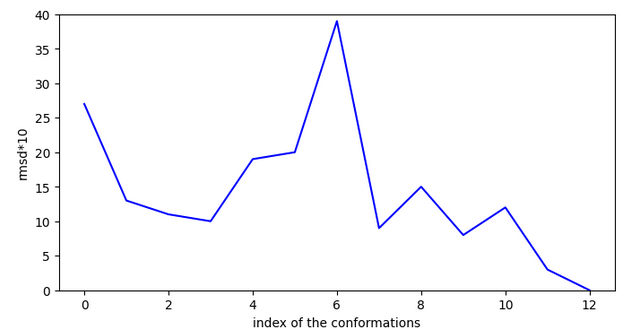
10 OK
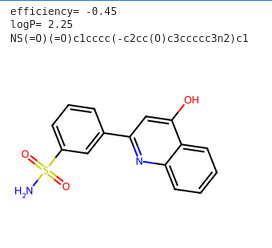
NS(=O)(=O)c1cccc(-c2cc(O)c3ccccc3n2)c1
A priori très facile à synthétiser.
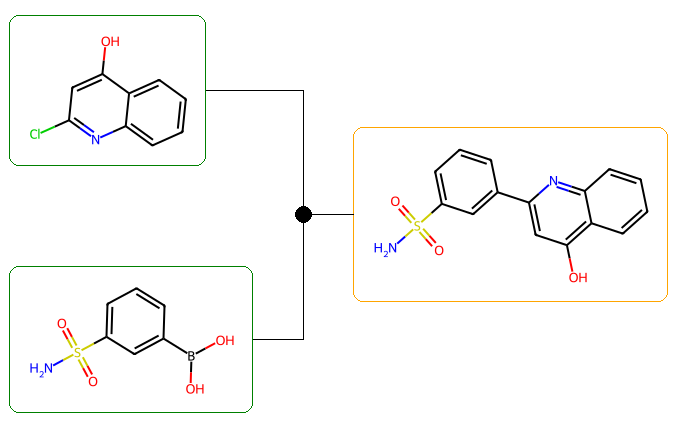
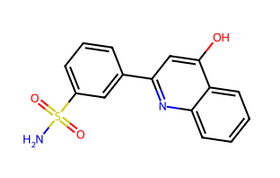
NS(=O)(=O)c1cccc(-c2cc(O)c3ccccc3n2)c1
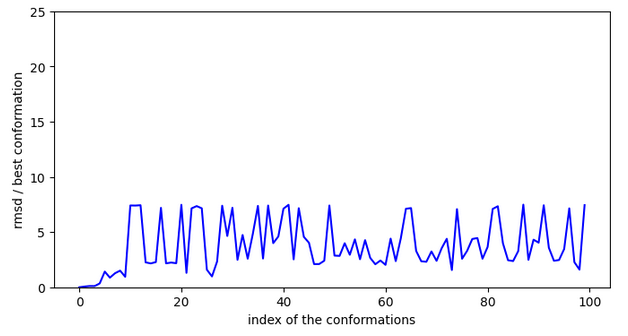
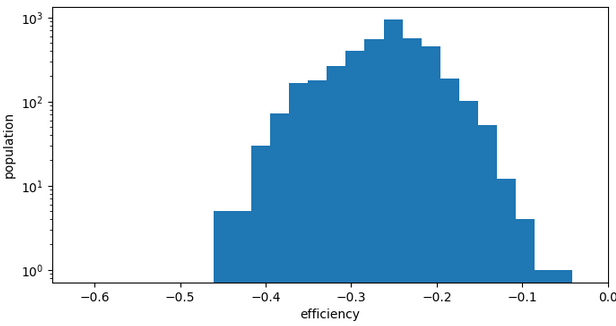
Chemin 1:

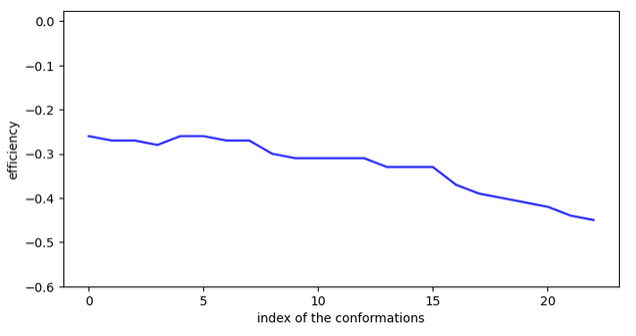
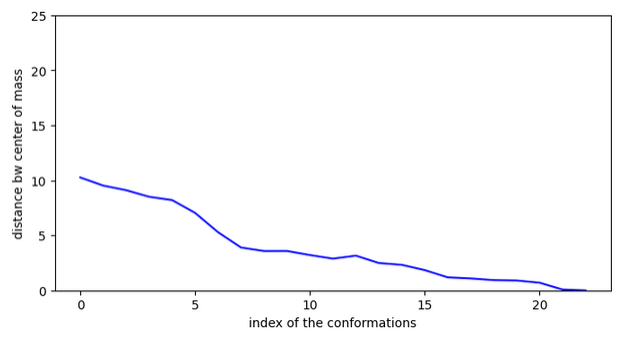
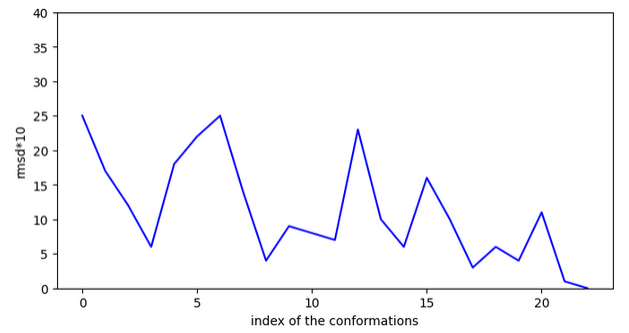
11 OK
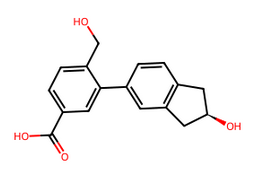
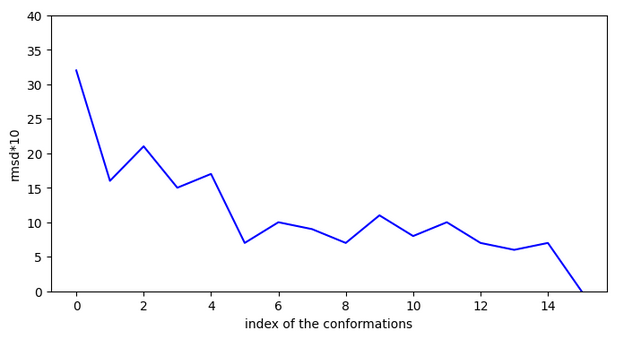
O=C(O)c1ccc(CO)c(-c2ccc3c(c2)C[C@H](O)C3)c1
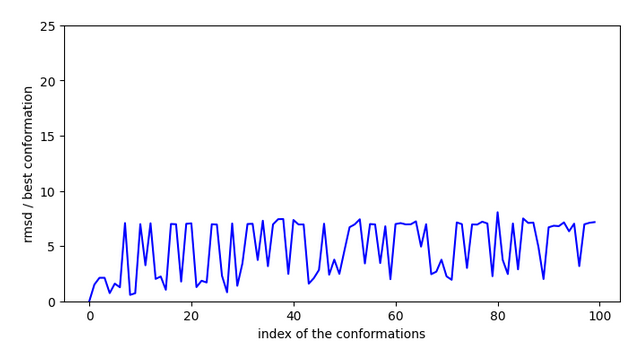
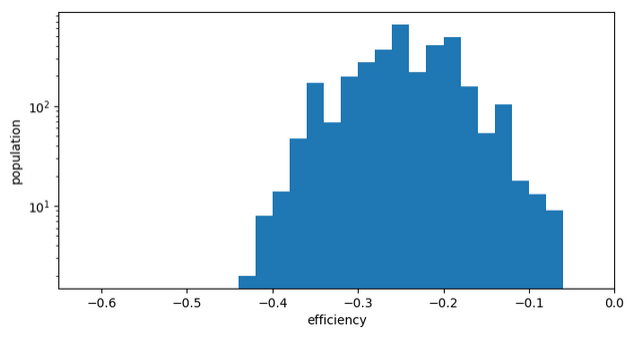
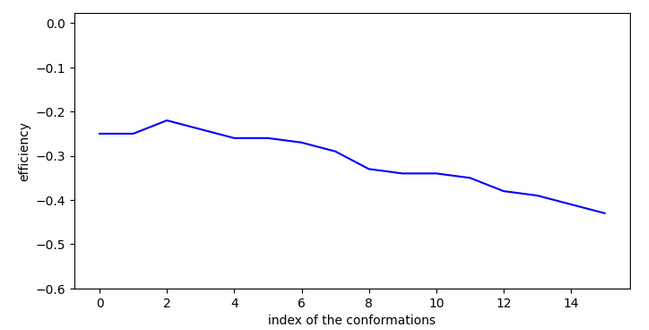
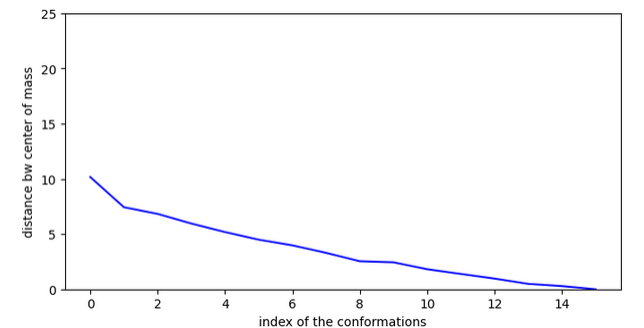
Chemin:

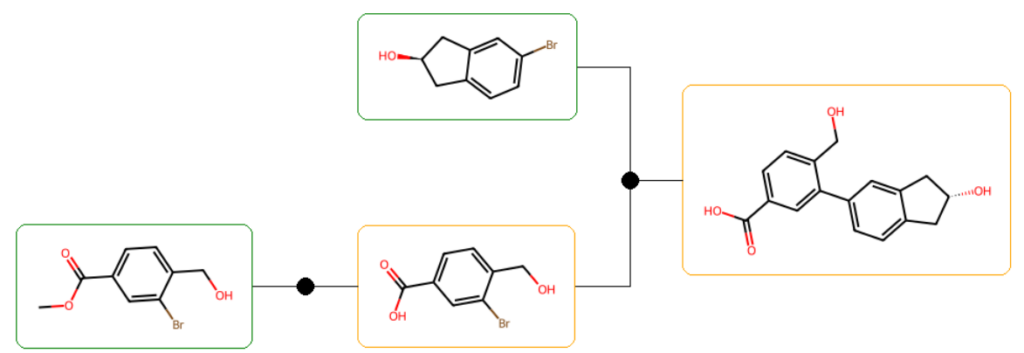
Rétrosynthèse.
12 OK
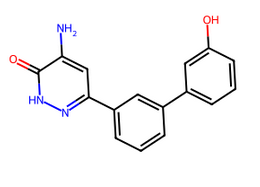
Nc1cc(-c2cccc(-c3cccc(O)c3)c2)n[nH]c1=O
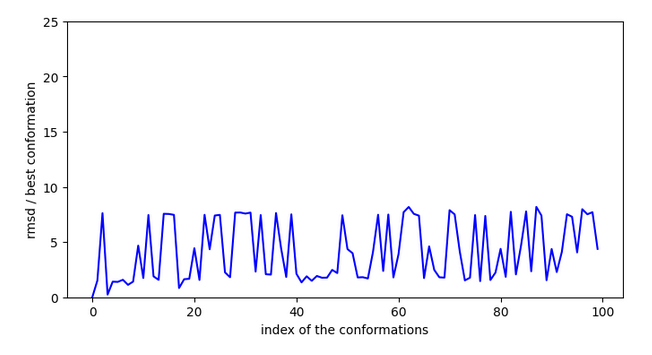
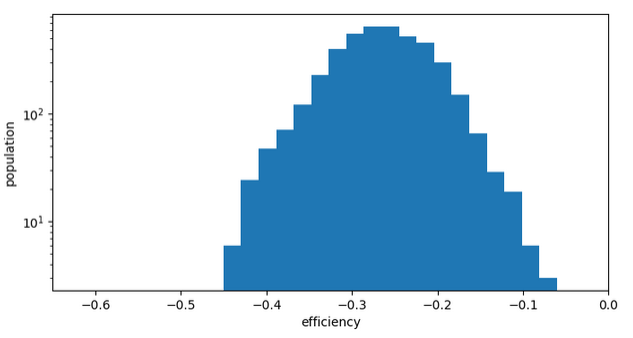

La 2ème solution comme point de départ donne un résultat parfait.
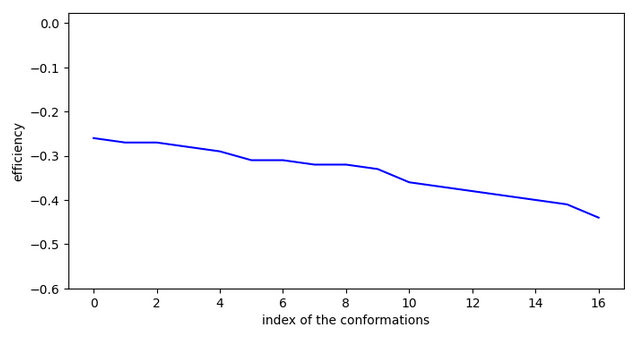
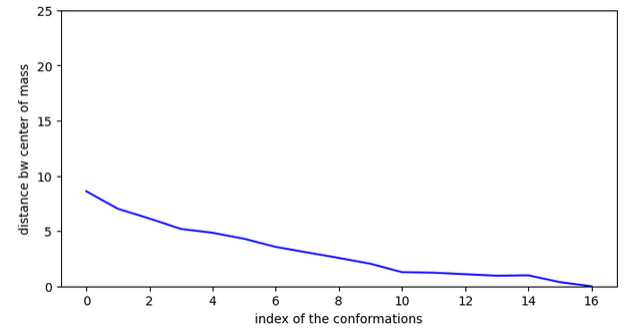
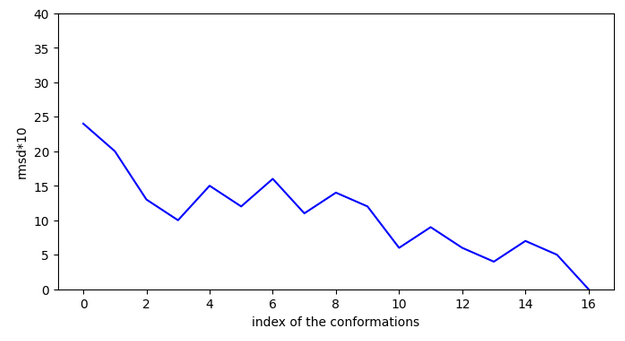
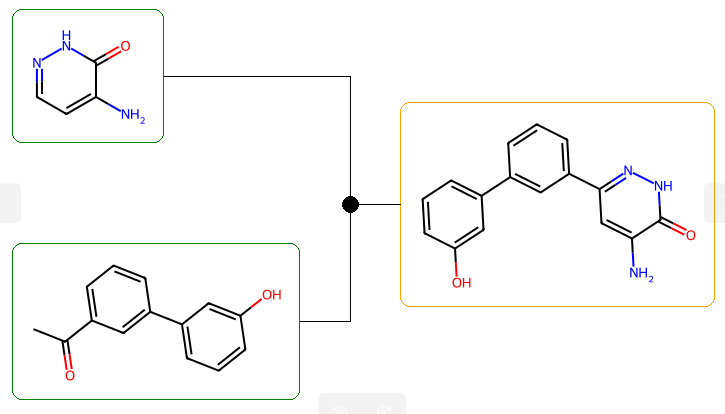
Rétrosynthèse.

